2023-06-01
上海璎黎药业林普利塞的多项研究结果于2023 EHA发表交流
第28届欧洲血液学协会大会(EHA)将于2023年6月8日至11日在德国法兰克福召开,欧洲血液学协会是欧洲最大的血液学组织。EHA致力于血液学的临床研究和实践,基础和转化,是血液领域一年一度的盛会。多年来,EHA的教育和科学计划强调最先进的临床实践,血液学研究的最新发现,以及关于血液病诊断和治疗的最新方法。本届EHA大会同样也涵盖了多个学科,并邀请行业极富盛名的专家和学者做主题演讲,是全球血液学家交流和互动的最佳时机。
2022 EHA年会公布了林普利塞治疗R/R FL患者的中国II期临床试验的最新数据,纳入至少接受过2次全身治疗的R/R FL患者,接受口服林普利塞80mg治疗,每日一次,结果显示,患者总缓解率(ORR)为79.8%,疾病控制率(DCR)高达96.6%,12个月OS率为91.4%;药物起效迅速,中位缓解时间为1.9个月;中位PFS为13.4个月,中位缓解持续时间(DOR)为12.3个月,林普利塞疗效持久,有效地延长了患者生存,且安全性良好。
林普利塞R/R FL研究的进一步亚组分析结果,以及林普利塞联合GEMOX研究的亚组分析结果将在2023年EHA继续分享交流:
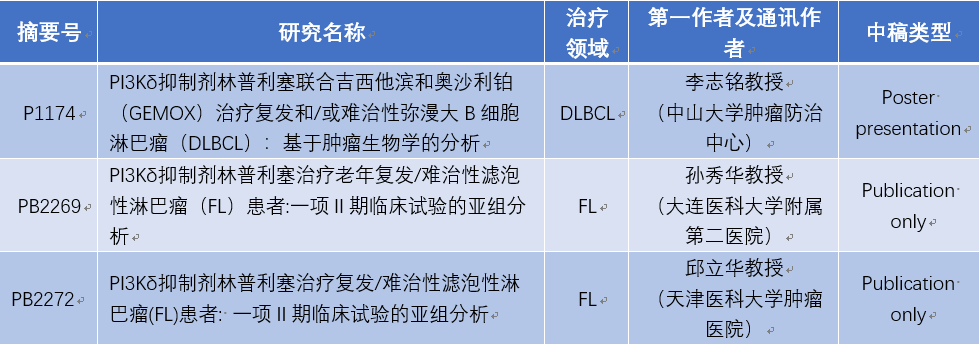
主要内容包括:
01
PI3Kδ抑制剂林普利塞联合吉西他滨和奥沙利铂(GEMOX)治疗复发和/或难治性弥漫大B细胞淋巴瘤(DLBCL):基于肿瘤生物学的分析
在GCB亚型(9例)与nonGCB亚型(25例)的受试者中,林普利塞的ORR分别为66.7%与 40%;DCR分别为77.8%和52.0%;中位PFS分别为3.0与5.3个月。
结论:基于肿瘤生物学的分析表明,与GCB型相比,林普利塞联合GEMOX对nonGCB型患者可能有更大的治疗获益趋势。
02
PI3Kδ抑制剂林普利塞治疗老年复发/难治性滤泡性淋巴瘤患者:一项Ⅱ期临床试验的亚组分析
在老年亚组(16例)与全年龄段(84例)复发/难治性滤泡性淋巴瘤受试者中,林普利塞的ORR分别为75%与79.8%,中位PFS分别为11.2与13.4个月。在老年受试者亚组中,OS达到1年的比率为100%。
结论:基于年龄亚组分析表明,对于老年复发难治性滤泡性淋巴瘤患者,林普利塞也显示出良好的疗效,这与年轻患者的结果相似。老年患者的总体安全性可控。
03
PI3Kδ抑制剂林普利塞治疗复发/难治性滤泡性淋巴瘤(FL)患者:一项Ⅱ期临床试验的亚组分析
在复发(39例)与难治性(45例)滤泡性淋巴瘤受试者中,ORR分别为87.2%与 73.3%;在最常见的≥3级的不良反应中,中性粒细胞减少的发生率分别为12.8%与17.8%;感染性肺炎的发生率分别为25.6%与13.3%;间质性肺病的发生率分别为0%与6.7%。
结论:基于复发/难治性亚组分析表明,林普利塞治疗复发FL患者的疗效在数值上优于难治性FL患者,但林普利塞在难治性FL中也显示出非常好的疗效,可为这类病人提供新的选择。
历尽天华成此景,踏过十年研发路,上海璎黎药业原研,中国首个全新一代高选择性PI3Kδ抑制剂林普利塞(商品名:因他瑞®)2022年11月正式获得中国国家药品监督管理局(NMPA)批准,用于治疗既往接受过至少两种全身系统治疗的复发或难治性(R/R)滤泡性淋巴瘤(FL)患者。2023年1月6日,由哈尔滨血液病肿瘤研究所马军教授和苏州大学附属第一医院吴德沛教授,开出了林普利塞首批处方,标志着因他瑞®正式进入临床应用,为我国R/R FL患者带来了全新的治疗选择!
“瑞”享新生,引“淋”未来,林普利塞获批上市后,璎黎药业与行业领军企业江苏恒瑞医药股份有限公司共同推动林普利塞在中国的商业化推广。恒瑞医药在中国拥有覆盖广泛的商业运营经验和临床开发能力,借助恒瑞医药成熟的市场推广体系,林普利塞将会有更多的机会为更多淋巴瘤患者带去生命的希望。

